Opioid
| Opioid | |
|---|---|
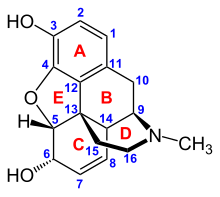
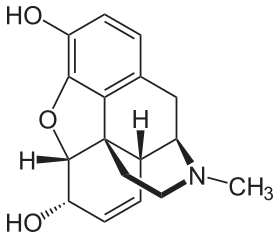 Prototipik opioid olan morfinin kimyasal yapısı.
| |
| İlaç sınıfı | |
| Sınıf tanımlayıcıları | |
| Amaç | Ağrı Kesici |
| ATC kodu | N02A |
| Etki modu | Opioid reseptörü |
| MeSH | D000701 |
| Vikiveri öğesi | |
Opioidler, morfin benzeri etkiler üretmek için opioid reseptörleri üzerinde etkili olan maddelerdir. Tıbbi olarak öncelikle anestezi de dahil olmak üzere ağrı kesici olarak kullanılırlar. Diğer tıbbi kullanımlar arasında ishalin baskılanması, opioid kullanım bozukluğu için replasman tedavisi, opioid doz aşımının tersine çevrilmesi ve öksürüğün bastırılması sayılabilir.Karfentanil gibi son derece güçlü opioidler sadece veteriner kullanımı için onaylanmıştır. Opioidler ayrıca öforik etkileri veya yoksunluk sendromunu önlemek için tıbbi olmayacak şekilde de sıklıkla kullanılır. Opioidler ölüme neden olabilir ve Amerika Birleşik Devletleri'nde infazlar için kullanılmıştır.
Opioidlerin yan etkileri kaşıntı, sedasyon, mide bulantısı, solunum depresyonu, kabızlık ve öfori içerebilir. Uzun süreli kullanım toleransa neden olabilir, yani aynı etkiyi elde etmek için artan dozların gerekli olduğu anlamına gelir ve fiziksel bağımlılık, ilacın aniden kesilmesinin hoş olmayan yoksunluk semptomlarına yol açtığı anlamına gelir. Öfori rekreasyonel kullanımı çeker ve opioidlerin rekreasyonel kullanımının sık sık, artan rekreasyonel kullanımı tipik olarak bağımlılıkla sonuçlanır. Benzodiazepinler gibi diğer depresan ilaçlarla aşırı dozda veya eşzamanlı kullanım genellikle solunum depresyonundan ölümle sonuçlanır.
Opioidler, esas olarak merkezi ve periferik sinir sisteminde ve gastrointestinal sistemde bulunan opioid reseptörlerine bağlanarak etki eder. Bu reseptörler, opioidlerin hem psikoaktif hem de somatik etkilerine aracılık eder. Opioid ilaçlar, ishal önleyici ilaç loperamid gibi kısmi agonistleri ve opioid kaynaklı kabızlık için naloksegol gibi antagonistleri içerir; bunlar kan-beyin bariyerini geçmez, ancak diğer opioidlerin bu reseptörlere bağlanmasını engelleyebilir.
Opioidler bağımlılık yaptığından ve ölümcül doz aşımına neden olabileceğinden, çoğu kontrollü maddelerdir. 2013 yılında, 28 ile 38 milyon insan opioidleri yasa dışı olarak kullandı (15 ile 65 yaş arasındaki küresel nüfusun %0,6 ile %0,8'i). 2011 yılında, Amerika Birleşik Devletleri'nde tahmini 4 milyon insan opioidleri rekreasyonel olarak kullandı veya onlara bağımlıydı. 2015 itibarıyla, artan rekreasyonel kullanım ve bağımlılık oranları, opioid ilaçların aşırı reçetelenmesine ve ucuz yasadışı eroine bağlanmaktadır. Tersine, aşırı reçeteleme, abartılı yan etkiler ve opioidlerden bağımlılık konusundaki korkular benzer şekilde ağrının yetersiz tedavisi için suçlanmaktadır.
Terminoloji
Opioidler, morfinin kendisi de dahil olmak üzere afyondan türetilen bu tür ilaçları ifade eden eski bir terim olan opiatları içerir. Diğer opioidler hidrokodon, oksikodon ve fentanil gibi yarı sentetik ve sentetik ilaçlardır; nalokson gibi antagonist ilaçlar ve endorfinler gibi endojen peptitlerdir.Afyon ve narkotik terimleri bazen opioid ile eş anlamlı olarak karşımıza çıkmaktadır. Afyon, afyon haşhaşının reçinesinde bulunan doğal alkaloidlerle sınırlıdır, ancak bazıları yarı sentetik türevleri içerir. Amerikan yasal terimi olarak 'uyuşukluk' veya 'uyku' anlamına gelen kelimelerden türetilen narkotik, kokain ve opioidleri ve bunların kaynak materyallerini ifade eder; ayrıca herhangi bir yasadışı veya kontrollü psikoaktif ilaca gevşek bir şekilde uygulanır. Bazı yargı bölgelerinde kontrol edilen tüm uyuşturucular yasal olarak uyuşturucu olarak sınıflandırılmıştır. Terim aşağılayıcı çağrışımlara sahip olabilir ve bu durumda kullanımı genellikle önerilmez.
Tıbbi kullanımlar
Ağrı
Zayıf opioid kodein, düşük dozlarda ve bir veya daha fazla başka ilaçla birlikte, hafif ağrıları tedavi etmek için reçeteli ilaçlarda ve reçetesiz olarak yaygın olarak bulunur. Diğer opioidler genellikle orta ile şiddetli ağrıların giderilmesi için kullanılır.
Akut ağrı
Opioidler akut ağrının tedavisinde etkilidir (ameliyat sonrası ağrı gibi). Orta ile şiddetli akut ağrının hızlıca giderilmesi için, opioidler hızlı başlangıçları, etkinlikleri ve azalmış bağımlılık riskleri nedeniyle sıklıkla tercih edilen tedavidir. Bununla birlikte, yeni bir rapor, ameliyat veya travma sonrası akut ağrı yönetimi için opioid analjezikler başlatıldığında uzun süreli opioid kullanımı için açık bir risk göstermiştir. Ayrıca, palyatif bakımda, kanser gibi bazı terminal durumlarda ve romatoid artrit gibi dejeneratif durumlarda ortaya çıkabilecek şiddetli, kronik, sakat bırakıcı ağrıya yardımcı olmak için önemli oldukları bulunmuştur. Birçok durumda opioidler, kronik kanser ağrısı olanlar için başarılı bir uzun vadeli bakım stratejisidir.
ABD'deki tüm eyaletlerin yarısından biraz fazlası, akut ağrı için opioidlerin reçete edilmesini veya dağıtılmasını kısıtlayan yasalar çıkarmıştır.
Kronik kanser dışı ağrı
Kılavuzlar, opioid riskinin, baş ağrısı, sırt ağrısı ve fibromiyalji dahil olmak üzere kanser dışı kronik durumların çoğu için kullanıldığında faydalarından daha büyük olduğunu öne sürmüştür. Bu nedenle kronik kanser dışı ağrılarda dikkatli kullanılmalıdırlar. Kullanılırsa fayda ve zararlar en az üç ayda bir yeniden değerlendirilmelidir.
Kronik ağrının tedavisinde, opioidler, parasetamol/asetaminofen, ibuprofen veya naproksen gibi NSAID'ler dahil olmak üzere diğer daha az riskli ağrı kesiciler düşünüldükten sonra denenecek bir seçenektir.Fibromiyalji veya migrenin neden olduğu ağrı da dahil olmak üzere bazı kronik ağrı türleri, tercihen opioidler dışındaki ilaçlarla tedavi edilir. Kronik nöropatik ağrıyı azaltmak için opioidlerin kullanılmasının etkinliği belirsizdir.
Opioidler baş ağrısı için birinci basamak tedavi olarak kontrendikedir, çünkü uyanıklığı bozar, bağımlılık riski taşır ve epizodik baş ağrılarının kronikleşme riskini arttırır. Opioidler ayrıca baş ağrısı ağrısına karşı duyarlılığın artmasına neden olabilir. Diğer tedaviler başarısız olduğunda veya kullanılamadığında, hasta kronik baş ağrısının gelişmesini önlemek için izlenebilirse opioidler baş ağrısı tedavisi için uygun olabilir.
Opioidler malign olmayan kronik ağrıların tedavisinde daha sık kullanılmaktadır. Bu uygulama günümüzde bağımlılık ve opioidlerin kötüye kullanımı ile ilgili yeni ve büyüyen bir soruna yol açmıştır. Çeşitli olumsuz etkiler nedeniyle, kronik ağrının uzun süreli yönetimi için opioidlerin kullanımı, diğer daha az riskli ağrı kesicilerin etkisiz bulunmadığı sürece endike değildir. Sinir ağrısı, migren ve fibromiyalji gibi sadece periyodik olarak ortaya çıkan kronik ağrı, sıklıkla opioidler dışındaki ilaçlarla daha iyi tedavi edilir. Parasetamol, ibuprofen ve naproksen dahil olmak üzere steroid olmayan antiinflamatuar ilaçlar daha güvenli alternatifler olarak kabul edilir. Sıklıkla oksikodon (Percocet) ile kombine parasetamol ve hidrokodon (Vicoprofen) ile kombine ibuprofen gibi opioidlerle birlikte kullanılırlar, bu da ağrı kesimini arttırır, ancak aynı zamanda rekreasyonel kullanımı caydırmayı amaçlar.
Diğer
Öksürük
Kodein bir zamanlar öksürük bastırıcılarda "altın standart" olarak görülüyordu, ancak bu pozisyonu günümüzde sorgulanmaktadır. Son zamanlarda yapılan bazı plasebo kontrollü çalışmalar, çocuklarda akut öksürük de dahil olmak üzere bazı nedenlerden dolayı plasebodan daha iyi olmayabileceğini bulmuştur. Bu nedenle çocuklar için önerilmez. Ek olarak, hidrokodonun çocuklarda yararlı olduğuna dair bir kanıt yoktur. Benzer şekilde 2012 Hollanda kılavuzu, akut öksürüğün tedavisi ile ilgili kullanımını önermemektedir. (Uzun zamandır kodein kadar etkili bir öksürük bastırıcı olduğu iddia edilen opioid analog dekstrometorfan benzer şekilde birkaç yeni çalışmada çok az fayda göstermiştir.)
Düşük doz morfin kronik öksürüğe yardımcı olabilir, ancak kullanımı yan etkilerle sınırlıdır.
İshal ve kabızlık
İshal baskın irritabl bağırsak sendromu vakalarında, ishali baskılamak için opioidler kullanılabilir. Loperamid, ishali baskılamak için kullanılan reçetesiz olarak kullanılabilen periferik olarak seçici bir opioiddir.
İshali bastırma yeteneği, opioidler birkaç haftadan fazla kullanıldığında kabızlık da üretir. Periferik olarak seçici bir opioid antagonisti olan Naloksegol, opioid kaynaklı kabızlığı tedavi etmek için artık mevcuttur.
Nefes darlığı
Opioidler, özellikle kanser ve KOAH gibi ileri seviye hastalıklarda nefes darlığına yardımcı olabilir. Bununla birlikte, yakın zamanda yapılan iki sistematik literatür incelemesinden elde edilen bulgular, opioidlerin ilerlemiş kanserli hastalarda nefes darlığı tedavisinde mutlaka daha etkili olmadığını ortaya koymuştur.
Hiperaljezi
Opioid kaynaklı hiperaljezi (OIH), kronik opioid maruziyetinden sonraki hastalarda belirgindir.
Yan etkiler
Diğer
- Bilişsel etkiler
- Opioid bağımlılığı
- Baş dönmesi
- İştah kaybı
- Gecikmiş mide boşalması
- Azalmış cinsel dürtü
- Cinsel işlev bozukluğu
- Testosteron seviyelerinde azalma
- Depresyon
- Bağışıklık yetmezliği
- Artan ağrı hassasiyeti
- Düzensiz menstrüasyon
- Düşme riskinde artış
- Yavaş nefes alma
- Koma
Her yıl dünya çapında 69.000 kişi aşırı doz opioid kullanımı nedeniyle ölmekte ve 15 milyon kişi opioid bağımlılığına sahiptir.
Yaşlı yetişkinlerde, opioid kullanımı "sedasyon, bulantı, kusma, kabızlık, idrar retansiyonu ve düşmeler" gibi artan yan etkilerle ilişkilidir. Sonuç olarak, opioid alan yaşlı yetişkinlerin yaralanma riski daha fazladır. Opioidler, aspirin ve parasetamol gibi diğer birçok ilacın aksine herhangi bir spesifik organ toksisitesine neden olmaz. Üst gastrointestinal kanama ve böbrek toksisitesi ile ilişkili değildirler.
Akut bel ağrısı ve osteoartrit tedavisi için opioidlerin reçete edilmesi uzun vadeli olumsuz etkilere sahip gibi görünmektedir.
USCDC'ye göre, metadon 1999-2010 yılları arasında ABD'de opioid bağlantılı ölümlerin %31'inde ve diğer opioidlerden çok daha yüksek oranda, tek uyuşturucu olarak %40'ında yer almıştır. Uzun süreli opioid çalışmaları, birçoğunun onları durdurduğunu ve küçük yan etkilerin yaygın olduğunu bulmuştur. Bağımlılık yaklaşık %0.3 oranında gerçekleşti. Amerika Birleşik Devletleri'nde 2016 yılında opioid doz aşımı, 10.000 kişiden 1,7'sinin ölümüyle sonuçlandı.
Aşağıdaki ABD tablolarında birçok ölüm birden fazla opioidi içermektedir:
ABD'de tüm opioid ilaçlardan kaynaklanan yıllık ölümler. Bu sayıya opioid analjezikler ile birlikte eroin ve yasadışı sentetik opioidler de dahildir.
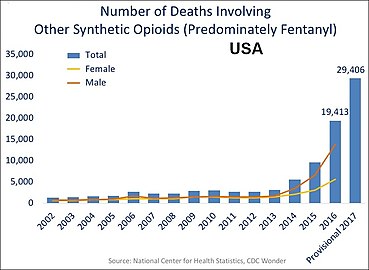
ABD'de ağırlıklı olarak Fentanil olmak üzere diğer sentetik opioidleri içeren yıllık ölümler.
Takviye bozuklukları
Tolerans
Tolerans, ilaç etkilerinin azalmasıyla sonuçlanan nöroadaptasyonlarla karakterize edilen bir süreçtir. Reseptör yukarı regülasyonu sıklıkla önemli bir rol oynayabilirken, diğer mekanizmalar da bilinmektedir. Tolerans, bazı etkiler için diğerlerinden daha belirgindir; Duygudurum, kaşıntı, idrar retansiyonu ve solunum depresyonu üzerindeki etkilere karşı tolerans yavaş gelişir, ancak analjezi ve diğer fiziksel yan etkilere karşı daha çabuk oluşur. Bununla birlikte, kabızlık veya miyoz (gözbebeğinin iki milimetreye eşit veya daha az daralması) için tolerans gelişmez. Bununla birlikte, bazı yazarlar toleransın miyozise dönüştüğünü ileri sürerek bu fikre meydan okunmuştur.
Opioidlere tolerans, aşağıdakiler de dahil olmak üzere bir dizi madde tarafından azaltılır:
- Kalsiyum kanal blokerleri
- İntratekal magnezyum ve çinko
- Dekstrometorfan, ketamin ve memantin gibi NMDA antagonistleri.
- Proglumid gibi kolesistokinin antagonistleri
- Fosfodiesteraz inhibitörü ibudilast gibi daha yeni ajanlar da bu uygulama için araştırılmıştır.
Tolerans, vücudun sıklıkla mevcut olan bir ilaca uyum sağladığı ve genellikle aynı etkiyi elde etmek için zaman içinde aynı ilacın daha yüksek dozlarını gerektirdiği fizyolojik bir süreçtir. Uzun süreler boyunca yüksek dozda opioid alan kişilerde sık görülen bir durumdur, ancak kötüye kullanım veya bağımlılık ile herhangi bir ilişki öngörmemektedir.
Fiziksel bağımlılık
Fiziksel bağımlılık, vücudun bir maddenin, bu durumda opioid ilacının varlığına fizyolojik adaptasyonudur. Madde kesildiğinde, doz aniden azaltıldığında veya özellikle opioidler söz konusu olduğunda, bir antagonist (örn. nalokson) veya bir agonist-antagonist (örn. pentazosin) uygulandığında yoksunluk semptomlarının gelişmesi ile tanımlanır. Fiziksel bağımlılık, bazı ilaçların normal ve beklenen bir yönüdür ve mutlaka hastanın bağımlı olduğu anlamına gelmez. Opiatlar için yoksunluk belirtileri, şiddetli disfori, başka bir afyon dozu için özlem, sinirlilik, terleme, bulantı, burun akıntısı, titreme, kusma ve kas ağrısını içerebilir. Opioid alımını günler ve haftalar içinde yavaş yavaş azaltmak, yoksunluk semptomlarını azaltabilir veya ortadan kaldırabilir. Çekilme hızı ve şiddeti, opioidin yarı ömrüne bağlıdır; eroin ve morfin yoksunluğu metadon yoksunluğundan daha hızlı gerçekleşir. Akut yoksunluk evresini genellikle aylarca sürebilen uzun süreli bir depresyon ve uykusuzluk evresi takip eder. Opioid yoksunluğu semptomları, klonidin gibi diğer ilaçlarla tedavi edilebilir. Fiziksel bağımlılık, uyuşturucu kötüye kullanımını veya gerçek bağımlılığı öngörmez ve toleransla aynı mekanizma ile yakından ilişkilidir. İbogain ile ilgili anekdotsal fayda iddiaları olsa da madde bağımlılığında kullanımını destekleyen veriler yetersizdir.
Düzenli dozlarda opioid alan kritik hastalar, sık görülen bir sendrom olarak iyatrojenik yoksunluk yaşarlar.
Bağımlılık
Uyuşturucu bağımlılığı, tipik olarak belirli ilaçların yanlış kullanımıyla ilişkili, zamänla ve daha yüksek ilaç dozajlarıyla gelişen karmaşık bir dizi davranıştır. Bağımlılık, etkilenen kişinin tehlikeli veya sağlıksız sonuçlara yol açan eylemlerde ısrar ettiği ölçüde psikolojik zorlamayı içerir. Opioid bağımlılığı, tıbbi nedenlerle reçete edildiği gibi ağızdan opioid almak yerine, insuflasyonu veya enjeksiyonu içerir.
Avusturya, Bulgaristan ve Slovakya gibi Avrupa ülkelerinde, buprenorfin veya metadonun yan etkilerini iyi tolere edemeyen hastalar için opiat ikame tedavisinde (OİT) yavaş salınımlı oral morfin formülasyonları kullanılmaktadır. Buprenorfin, bağımlılığın daha uzun süreli tedavisi için nalokson ile birlikte de kullanılabilir. Birleşik Krallık da dahil olmak üzere diğer Avrupa ülkelerinde bu, değişen bir kabul ölçeğinde olsa da OİT için yasal olarak kullanılmaktadır.
Yavaş salınan ilaç formülasyonları, ağrı hastalarına hala meşru ağrı kesici ve kullanım kolaylığı sağlamaya çalışırken, kötüye kullanımı engellemeyi ve bağımlılık oranlarını düşürmeyi amaçlamaktadır. Bununla birlikte, bu tür müstahzarların etkinliği ve güvenliği hakkında sorular devam etmektedir. Daha fazla kurcalamaya dayanıklı ilaçlar şu anda FDA tarafından pazar onayı için denemeler ile değerlendirilmektedir.
Mevcut kanıt miktarı yalnızca zayıf bir sonuca varılmasına izin verir, ancak madde kullanım bozukluğu öyküsü olmayan hastalarda opioid kullanımını uygun şekilde yöneten bir doktorun, bağımlılık geliştirme veya diğer ciddi yan etkiler açısından çok az riskle uzun süreli ağrı kesici sağlayabileceğini düşündürür.
Opioidlerle ilgili sorunlar şunları içerir:
- Bazı insanlar opioidlerin tüm ağrılarını gidermediğini fark edebilirler.
- Bazı insanlar, opioidlerin yan etkilerinin, terapinin yararından daha ağır basan sorunlara yol açtığını düşünebilirler.
- Bazı insanlar zamanla opioidlere tolerans geliştirir. Bu, faydayı sürdürmek için ilaç dozlarını artırmalarını gerektirir ve bu da istenmeyen yan etkileri artırır.
- Uzun süreli opioid kullanımı, hastanın ağrıya duyarlılığının arttığı bir durum olan opioid kaynaklı hiperaljeziye neden olabilir.
Tüm opioidler yan etkilere neden olabilir. Ağrıyı gidermek için opioid alan hastalarda sık görülen yan etkiler bulantı ve kusma, uyuşukluk, kaşıntı, ağız kuruluğu, baş dönmesi ve kabızlığı içerir.
Mide bulantısı ve kusma belirtileri
Bulantıya tolerans, antiemetiklerin (örneğin, gece bir kez düşük doz haloperidol) çok etkili olduğu 7-10 gün içinde ortaya çıkar. Tardif diskinezi gibi ciddi yan etkiler nedeniyle haloperidol artık nadiren kullanılmaktadır. Benzer risklere sahip olmasına rağmen, ilgili bir ilaç olan proklorperazin daha sık kullanılır. Ondansetron veya tropisetron gibi daha güçlü antiemetikler, daha yüksek maliyetlerine rağmen, bazen bulantı şiddetli veya sürekli ve rahatsız edici olduğunda kullanılır. Daha ucuz bir alternatif, domperidon ve metoklopramid gibi dopamin antagonistleridir. Domperidon kan-beyin bariyerini geçmez ve ters merkezi antidopaminerjik etkiler üretmez, ancak kemoreseptör tetikleme bölgesindeki opioid emetik etkisini bloke eder. (İlaç ABD'de mevcut değildir) Antikolinerjik özelliklere sahip bazı antihistaminikler (örneğin orfenadrin veya difenhidramin) de etkili olabilir. Birinci nesil antihistamin hidroksizin, hareket bozukluklarına neden olmaması ve ayrıca analjezik koruyucu özelliklere sahip olması gibi ek avantajlarla birlikte çok yaygın olarak kullanılmaktadır. Δ9-tetrahidrokanabinol bulantı ve kusmayı giderir; aynı zamanda daha düşük dozlarda opioid kullanımına izin veren, bulantı ve kusmayı azaltan analjezi üretir.
- 5-HT3 antagonistleri (örn. ondansetron)
- Dopamin antagonistleri (örn. domperidon)
- Antikolinerjik antihistaminikler (örn. difenhidramin)
- Δ9-tetrahidrokanabinol (örn. dronabinol)
Kusma, beynin kusma merkezi olan postrema bölgesinin kemoreseptör tetikleyici bölgesi üzerindeki doğrudan etkinin yanı sıra, gastrik stazdan (büyük hacimli kusma, kusmayla geçen kısa süreli mide bulantısı, özofagal reflü, epigastrik dolgunluk, erken doyma) kaynaklanır. Kusma böylece prokinetik ajanlar (örn. domperidon veya metoklopramid) tarafından önlenebilir. Kusma zaten başlamışsa bu ilaçların oral olmayan bir yolla (örn. metoklopramid için subkutan, domperidon için rektal yoldan) uygulanması gerekir.
- Prokinetik ajanlar (örn. domperidon)
- Antikolinerjik ajanlar (örn. orfenadrin)
Kanıtlar, opioid içeren anestezinin postoperatif bulantı ve kusma ile ilişkili olduğunu göstermektedir.
Opioid kullanan kronik ağrısı olan hastalarda ağrıda ve fiziksel işlevde küçük iyileşmeler ve kusma riskinde artış olmuştur.
Somnolans
Somnolans toleransı genellikle 5-7 gün içinde gelişir, ancak zahmetliyse alternatif bir opioide geçmek genellikle yardımcı olur. Fentanil, morfin ve diamorfin (eroin) gibi belirli opioidler özellikle yatıştırıcı olma eğilimindeyken; oksikodon, tilidin ve meperidin (petidin) gibi diğerleri nispeten daha az sedasyon üretme eğilimindedir, ancak bireysel hastaların yanıtları belirgin şekilde değişebilir ve bir dereceye kadar deneme ve belirli bir hasta için en uygun ilacı bulmak için hata gerekebilir. Aksi takdirde, CNS uyarıcıları ile tedavi genellikle etkilidir.
- Uyarıcılar (örn. kafein, modafinil, amfetamin, metilfenidat)
Kaşıntı
Ağrıyı gidermek için opioidler kullanıldığında kaşıntı ciddi bir sorun olmama eğilimindedir, ancak antihistaminikler, ortaya çıktığında kaşıntıya karşı koymak için yararlıdır. Feksofenadin gibi yatıştırıcı olmayan antihistaminikler, opioid kaynaklı uyuşukluğun artmasını engelledikleri için sıklıkla tercih edilir. Bununla birlikte, orfenadrin gibi bazı yatıştırıcı antihistaminikler, daha küçük dozlarda opioidlerin kullanılmasına izin veren sinerjik bir ağrı giderici etki üretebilir. Sonuç olarak, Meprozin (meperidin/prometazin) ve Diconal (dipipanon/siklizin) gibi çeşitli opioid/antihistaminik kombinasyon ürünleri pazarlanmıştır ve bunlar aynı zamanda opioid kaynaklı mide bulantısını da azaltabilir.
- Antihistaminikler (örneğin feksofenadin)
Kabızlık
Opioid kaynaklı kabızlık (OKK), uzun süreli opioid alan kişilerin %90 ile 95'inde gelişir. Bu soruna tolerans genellikle gelişmediğinden, uzun süreli opioid kullanan çoğu kişinin müshil veya lavman alması gerekir.
OKK tedavisi ardışıktır ve ciddiyete bağlıdır. İlk tedavi şekli farmakolojik değildir ve diyet lifi, sıvı alımı (günde yaklaşık 15 L) ve fiziksel aktivite gibi yaşam tarzı değişikliklerini içerir. Farmakolojik olmayan önlemler etkisiz ise, dışkı yumuşatıcılar (örn. polietilen glikol), yığın oluşturan laksatifler (örn. lif takviyeleri), uyarıcı laksatifler (örn. bisakodil, senna) ve/veya lavman dahil laksatifler kullanılabilir. OKK için yaygın bir müshil rejimi, docusate ve bisakodil kombinasyonudur. Ozmotik laksatifler, laktuloz, polietilen glikol ve magnezyum sütü (magnezyum hidroksit) ve ayrıca mineral yağ (bir yağlayıcı müshil) de yaygın olarak kullanılır.
Laksatifler yeterince etkili değilse (ki bu genellikle böyledir),metilnaltrekson bromür, naloksegol, alvimopan veya nalokson (oksikodon/naloksonda olduğu gibi) gibi periferik olarak seçici bir opioid antagonisti içeren opioid formülasyonları veya rejimleri denenebilir. Bir 2018 Cochrane incelemesi, kanıtların alvimopan, nalokson veya metilnaltrekson bromür için geçici olduğunu bulmuştur. Ağız yoluyla Nalokson güncellemesi en etkili gibi görünmektedir. Günlük 0,2 mg naldemedin dozunun, OKK hastalarında semptomları önemli ölçüde iyileştirdiği gösterilmiştir.
Opioid rotasyonu, uzun süreli kullanıcılarda kabızlığın etkisini en aza indirmek için önerilen bir yöntemdir. Tüm opioidler kabızlığa neden olurken, ilaçlar arasında bazı farklılıklar vardır; çalışmalar, tramadol, tapentadol, metadon ve fentanilin nispeten daha az kabızlığa neden olabileceğini düşündürürken, kodein, morfin, oksikodon veya hidromorfon ile kabızlık nispeten daha şiddetli olabilir.
Solunum depresyonu
Solunum depresyonu, opioid kullanımıyla ilişkili en ciddi advers reaksiyondur, ancak genellikle opioid kullanmamış bir hastada tek bir intravenöz dozun kullanımıyla görülür. Ağrıyı gidermek için düzenli olarak opioid alan hastalarda solunum depresyonuna tolerans hızla oluşur, bu nedenle klinik bir sorun değildir. Solunum depresyonunu kısmen bloke edebilen birkaç ilaç geliştirilmiştir, ancak şu anda bu amaç için onaylanmış tek solunum uyarıcısı, bu uygulamada yalnızca sınırlı etkinliğe sahip olan doksapramdır.BIMU8 ve CX-546 gibi daha yeni ilaçlar çok daha etkili olabilir.
- Solunum uyarıcıları: karotis kemoreseptör agonistleri (örn. doksapram), 5-HT4 agonistleri (örn. BIMU8), δ-opioid agonistleri (örn. BW373U86) ve AMPAkinler (örn. CX717) analjeziyi etkilemeden opioidlerin neden olduğu solunum depresyonunu azaltabilir, ancak bu ilaçların çoğu sadece orta derecede etkilidir veya insanlarda kullanımını engelleyen yan etkileri vardır. 8-OH-DPAT ve repinotan gibi 5-HT1A agonistleri de opioid kaynaklı solunum depresyonuna karşı koyar, ancak aynı zamanda analjeziyi azaltır, bu da bu uygulama için kullanışlılıklarını sınırlar.
- Opioid antagonistleri (örn. nalokson, nalmefen, diprenorfin)
Opioid uygulamasından sonraki ilk 24 saat, yaşamı tehdit eden solunum depresyonu açısından en kritik olan gibi görünmektedir, ancak opioid kullanımına daha dikkatli bir yaklaşımla önlenebilir olabilir.
Kardiyak, solunum hastalığı ve/veya obstrüktif uyku apnesi olan hastalar solunum depresyonu için yüksek risk altındadır.
Artan ağrı duyarlılığı
Opioid kaynaklı hiperaljezi - ağrıyı gidermek için opioid kullanan kişilerin paradoksal olarak bu ilacın bir sonucu olarak daha fazla ağrı yaşadığı - bazı insanlarda gözlenmiştir. Bu fenomen, nadir olmakla birlikte, palyatif bakım alan bazı kişilerde, çoğunlukla doz hızla artırıldığında görülür. Karşılaşılırsa, birkaç farklı opioid ağrı kesici ilaç arasında rotasyon, artan ağrı gelişimini azaltabilir. Opioid kaynaklı hiperaljezi daha çok kronik kullanımda veya kısa süreli yüksek dozlarda ortaya çıkar, ancak bazı araştırmalar bunun çok düşük dozlarda da ortaya çıkabileceğini düşündürmektedir.
Bazen nöropatik ağrının kötüleşmesine eşlik eden hiperaljezi ve allodini gibi yan etkiler, opioid analjeziklerle uzun süreli tedavinin sonuçları olabilir, özellikle de artan tolerans, zaman içinde etkinlik kaybına ve bunun sonucunda ilerleyen doz artışına neden olduğunda. Bu durum büyük ölçüde opioid ilaçların nosiseptin reseptörü, sigma reseptörü ve Toll benzeri reseptör 4 dahil olmak üzere üç klasik opioid reseptörü dışındaki hedeflerdeki etkilerinin bir sonucu gibi görünmektedir ve hayvan modellerinde sırasıyla J-113,397, BD-1047 veya (+)-nalokson gibi bu hedeflerdeki antagonistlerle önlenebilir. Günümüzde insanlarda opioid kaynaklı hiperaljeziye karşı koymak için özel olarak onaylanmış hiçbir ilaç yoktur ve ciddi vakalarda tek çözüm opioid analjeziklerin kullanımının kesilmesi ve bunların opioid olmayan analjezik ilaçlarla değiştirilmesi olabilir. Bununla birlikte, bu yan etkinin gelişimine karşı bireysel hassasiyet yüksek oranda doza bağlı olduğundan ve hangi opioid analjeziğin kullanıldığına bağlı olarak değişebileceğinden, birçok hasta opioid ilacın dozunu azaltarak (genellikle ek bir opioid olmayan analjezik ilavesiyle birlikte), farklı opioid ilaçlar arasında rotasyon yaparak veya nöropatik ağrıyı da önleyen karma etki tarzına sahip daha hafif bir opioide, özellikle tramadol veya tapentadole geçerek bu yan etkiden kaçınabilir.
- Ketamin gibi NMDA reseptör antagonistleri
- Milnasipran gibi SNRI'ler
- Gabapentin veya pregabalin gibi antikonvülzanlar
Diğer yan etkiler
Düşük cinsiyet hormonu seviyeleri
Klinik çalışmalar, tıbbi ve eğlence amaçlı opioid kullanımını farklı cinsiyetlerde hipogonadizm (düşük cinsiyet hormonu seviyeleri) ile tutarlı bir şekilde ilişkilendirmiştir. Bu etki doza bağlıdır. Çoğu çalışma, kronik opioid kullanıcılarının çoğunun (belki de %90'ının) hipogonadizm geliştirdiğini göstermektedir. 2015 yılında yapılan bir sistematik inceleme ve meta-analiz, opioid tedavisinin erkeklerde testosteron seviyelerini ortalama 165 ng/dL (5,7 nmol/L) kadar baskıladığını ve bunun da testosteron seviyesinde neredeyse %50'lik bir azalmaya neden olduğunu ortaya koymuştur. Buna karşılık, opioid tedavisi kadınlarda testosteron seviyelerini önemli ölçüde etkilememiştir. Bununla birlikte, opioidler lüteinizan hormon (LH) üretimini sınırlayarak kadınlarda menstrüasyona da müdahale edebilir. Opioid kaynaklı hipogonadizm, muhtemelen östradiol eksikliğine bağlı olarak opioid kullanımının osteoporoz ve kemik kırılması ile güçlü ilişkisine neden olmaktadır. Ayrıca ağrıyı artırabilir ve böylece opioid tedavisinin amaçlanan klinik etkisine müdahale edebilir. Opioid kaynaklı hipogonadizm muhtemelen hipotalamus ve hipofiz bezindeki opioid reseptörlerinin agonizminden kaynaklanmaktadır. Bir çalışma, eroin bağımlılarının depresif testosteron seviyelerinin yoksunluktan sonraki bir ay içinde normale döndüğünü, bu da etkinin kolayca geri döndürülebilir olduğunu ve kalıcı olmadığını düşündürmektedir. 2013 yılı itibarıyla, düşük doz veya akut opioid kullanımının endokrin sistem üzerindeki etkisi belirsizdir. Opioidlerin uzun süreli kullanımı diğer hormonal sistemleri de etkileyebilir.
İşin aksaması
Opioid kullanımı işe geri dönememe için bir risk faktörü olabilir.
Güvenlik açısından hassas herhangi bir görev yapan kişiler opioid kullanmamalıdır. Sağlık hizmeti sağlayıcıları, vinç veya forklift dahil ağır ekipman kullanan veya kullanan çalışanların kronik veya akut ağrıyı opioidlerle tedavi etmelerini önermemelidir. Güvenlik açısından hassas operasyonlar yürüten işçileri yöneten işyerleri, bu işçiler doktorları tarafından opioidlerle tedavi edildiği sürece işçileri daha az hassas görevlere vermelidir.
Opioidleri uzun süre alan kişilerin işsiz kalma olasılığı artmıştır. Opioid almak hastanın hayatını daha da bozabilir ve opioidlerin olumsuz etkileri hastaların aktif bir yaşam sürmeleri, iş bulmaları ve kariyer sürdürmeleri önünde önemli bir engel haline gelebilir.
Ek olarak, istihdam eksikliği, reçeteli opioidlerin anormal kullanımının bir göstergesi olabilir.
Artan kaza eğilimi
Opioid kullanımı kazaya yatkınlığı artırabilir. Opioidler trafik kazası ve kaza sonucu düşme riskini artırabilir.
Azaltılmış dikkat
Opioidlerin, antidepresanlar ve/veya antikonvülzanlarla birlikte kullanıldığında dikkati azalttığı gösterilmiştir.
Nadir yan etkiler
Ağrı kesici olarak opioid kullanan hastalarda seyrek görülen advers reaksiyonlar şunlardır: doza bağlı solunum depresyonu (özellikle daha güçlü opioidlerle), konfüzyon, halüsinasyonlar, deliriyum, ürtiker, hipotermi, bradikardi/taşikardi, ortostatik hipotansiyon, baş dönmesi, baş ağrısı, idrar retansiyonu, üreterik veya biliyer spazm, kas sertliği, miyoklonus (yüksek dozlarda) ve kızarma (histamin salınımına bağlı, fentanil ve remifentanil hariç). Opioidlerin hem terapötik hem de kronik kullanımı bağışıklık sisteminin işlevini tehlikeye atabilir. Opioidler makrofaj progenitör hücrelerin ve lenfositlerin çoğalmasını azaltır ve hücre farklılaşmasını etkiler (Roy & Loh, 1996). Opioidler ayrıca lökosit göçünü de engelleyebilir. Ancak bunun ağrının giderilmesi bağlamındaki önemi bilinmemektedir.
Etkileşimler
Opioidleri diğer ilaçlarla birlikte kullanan hastaları tedavi eden hekimler, daha ileri tedavinin endike olduğuna dair sürekli dokümantasyon tutarlar ve hastanın durumu daha az riskli tedaviyi hak edecek şekilde değişirse tedaviyi ayarlama fırsatlarının farkında olurlar.
Diğer depresan ilaçlarla birlikte
Opioidlerin benzodiazepinler veya etanol gibi diğer depresan ilaçlarla eşzamanlı kullanımı advers olay ve aşırı doz oranlarını artırmaktadır. Buna rağmen, opioidler ve benzodiazepinler birçok ortamda eşzamanlı olarak dağıtılmaktadır. Tek başına opioid doz aşımında olduğu gibi, bir opioid ve başka bir depresanın kombinasyonu solunum depresyonunu hızlandırabilir ve genellikle ölüme yol açabilir. Bu riskler, hasta davranışındaki ve tedaviye uyumdaki değişiklikler için sürekli tarama yapabilecek bir doktor tarafından yakın izleme ile azaltılır.
Opioid antagonisti
Opioid etkileri (olumsuz veya başka türlü) nalokson veya naltrekson gibi bir opioid antagonisti ile tersine çevrilebilir. Bu rekabetçi antagonistler opioid reseptörlerine agonistlerden daha yüksek afinite ile bağlanır ancak reseptörleri aktive etmez. Bu, agonistin yerini alarak agonist etkilerini zayıflatır veya tersine çevirir. Bununla birlikte, naloksonun eliminasyon yarı ömrü opioidin kendisinden daha kısa olabilir, bu nedenle tekrar dozlama veya sürekli infüzyon gerekebilir veya nalmefen gibi daha uzun etkili bir antagonist kullanılabilir. Düzenli olarak opioid alan hastalarda, dayanılmaz bir ağrıyla uyanmak gibi şiddetli ve üzücü bir reaksiyondan kaçınmak için opioidin sadece kısmen tersine çevrilmesi esastır. Bu, tam doz verilmeyip solunum hızı düzelene kadar küçük dozlarda verilerek sağlanır. Daha sonra bir infüzyon başlatılarak tersine çevirme bu seviyede tutulur ve ağrı kesilmeye devam edilir. Opioid antagonistleri, opioid aşırı dozunu takiben solunum depresyonu için standart tedavi olmaya devam etmektedir ve nalokson en yaygın kullanılanıdır, ancak daha uzun etkili antagonist nalmefen, metadon gibi uzun etkili opioidlerin aşırı dozlarını tedavi etmek için kullanılabilir ve diprenorfin, veteriner hekimlikte kullanılan etorfin ve karfentanil gibi son derece güçlü opioidlerin etkilerini tersine çevirmek için kullanılır. Bununla birlikte, opioid antagonistleri opioid analjeziklerin faydalı etkilerini de bloke ettiğinden, genellikle sadece aşırı doz tedavisinde faydalıdırlar; opioid antagonistlerinin yan etkileri azaltmak için opioid analjeziklerle birlikte kullanılması, dikkatli doz titrasyonu gerektirir ve analjezinin sürdürülmesine izin verecek kadar düşük dozlarda genellikle zayıf etkilidir.
Naltreksonun ciddi advers olay riskini artırmadığı görülmüştür, bu da oral naltreksonun güvenilirliğini doğrulamaktadır. Nalokson kullanan hastalarda rebound toksisitesine bağlı ölüm veya ciddi advers olaylar nadir görülmüştür.
Farmakoloji
| İlaç | Göreceli Potens |
İyonize Olmayan Oran | Bağlayıcı Protein | Lipid Çözünürlüğü |
|---|---|---|---|---|
| Morfin | 1 | ++ | ++ | ++ |
| Petidin (meperidin) | 0.1 | + | +++ | +++ |
| Hidromorfon | 10 | + | +++ | |
| Alfentanil | 10–25 | ++++ | ++++ | +++ |
| Fentanil | 75–125 | + | +++ | ++++ |
| Remifentanil | 250 | +++ | +++ | ++ |
| Sufentanil | 500–1000 | ++ | ++++ | ++++ |
| Etorfin | 1000–3000 | |||
| Karfentanil | 10000 |
Opioidler sinir sistemi ve diğer dokulardaki spesifik opioid reseptörlerine bağlanır. Opioid reseptörlerinin üç ana sınıfı vardır: μ, κ, δ (mu, kappa ve delta), ancak on yedi kadar reseptör bildirilmiştir ve ε, ι, λ ve ζ (Epsilon, Iota, Lambda ve Zeta) reseptörlerini içerir. Buna karşılık, σ (Sigma) reseptörleri artık opioid reseptörleri olarak kabul edilmemektedir çünkü aktivasyonları opioid ters-agonisti nalokson tarafından tersine çevrilmez, klasik opioidler için yüksek afiniteli bağlanma göstermezler ve diğer opioid reseptörleri levo-rotatori izomerler için stereo-seçici iken dekstro-rotatori izomerler için stereoselektiftirler. Buna ek olarak, μ-reseptörünün üç alt tipi vardır: μ1 ve μ2 ve yeni keşfedilen μ3. Klinik öneme sahip bir diğer reseptör de ağrı tepkilerinde rol oynayan ve analjezik olarak kullanılan μ-opioid agonistlerine karşı tolerans gelişiminde önemli bir role sahip olan opioid-reseptör benzeri reseptör 1'dir (ORL1). Bunların hepsi GABAerjik nörotransmisyon üzerinde etkili olan G-proteinine bağlı reseptörlerdir.
Bir opioide verilen farmakodinamik yanıt, opioidin bağlandığı reseptöre, bu reseptöre olan afinitesine ve opioidin bir agonist veya antagonist olmasına bağlıdır. Örneğin, opioid agonisti morfinin supraspinal analjezik özelliklerine μ1 reseptörünün aktivasyonu; μ2 reseptörü tarafından solunum depresyonu ve fiziksel bağımlılık; ve κ reseptörü tarafından sedasyon ve spinal analjezi aracılık eder. Her opioid reseptör grubu, reseptör alt tipleri (örneğin μ1 ve μ2 gibi) daha da [ölçülebilir] spesifik yanıtlar sağlayarak farklı bir dizi nörolojik yanıt ortaya çıkarır. Her opioid için benzersiz olan, çeşitli opioid reseptör sınıflarına farklı bağlanma afinitesidir (örneğin μ, κ ve δ opioid reseptörleri, opioidin spesifik reseptör bağlanma afinitelerine göre farklı büyüklüklerde aktive edilir). Örneğin, opiat alkaloid morfin μ-opioid reseptörüne yüksek afinite ile bağlanırken, ketazosin ĸ reseptörlerine yüksek afinite gösterir. Her biri kendine özgü etki profiline sahip bu kadar geniş bir opioid sınıfının ve moleküler tasarımların var olmasını sağlayan şey bu kombinasyonel mekanizmadır. Opioid metabolizmasından metabolik parçalanma (N-dealkilasyon gibi) sorumlu olduğu için, bireysel moleküler yapıları da farklı etki sürelerinden sorumludur.

Fonksiyonel seçicilik
Yeni bir ilaç geliştirme stratejisi, reseptör sinyal iletimini dikkate almaktadır. Bu strateji, istenmeyen yollar üzerindeki etkiyi azaltırken arzu edilen sinyal yollarının aktivasyonunu artırmaya çalışmaktadır. Bu farklı stratejiye işlevsel seçicilik ve yanlı agonizm gibi çeşitli isimler verilmiştir. Kasıtlı olarak yanlı agonist olarak tasarlanan ve klinik değerlendirmeye alınan ilk opioid oliseridin ilacıdır. Analjezik aktivite gösterir ve yan etkileri azaltır.
Opioid karşılaştırması
Opioidlerin göreceli etki gücünü karşılaştıran eşdeğerlik oranlarını belirlemek için kapsamlı araştırmalar yapılmıştır. Bir opioid dozu verildiğinde, bir diğerinin eşdeğer dozajını bulmak için bir ekanaljezik tablosu kullanılır. Bu tür tablolar opioid rotasyon uygulamalarında ve bir opioidi referans opioid olan morfinle karşılaştırarak tanımlamak için kullanılır. Eşdeğer ağrı kesici tabloları tipik olarak ilaç yarı ömürlerini ve bazen de morfin gibi uygulama yollarına göre aynı ilacın eşdeğer ağrı kesici dozlarını listeler: oral ve intravenöz.
Geçmiş
Doğal olarak oluşan opioidler
Opioidler dünyanın bilinen en eski ilaçları arasındadır. Bir insan arkeolojik alanında Papaver somniferum'un bilinen en eski kanıtı, M.Ö. 5.700-5.500 yılları arasındaki Neolitik döneme aittir. Tohumları İber Yarımadası'ndaki Cueva de los Murciélagos'ta ve İtalyan Yarımadası'ndaki La Marmotta'da bulunmuştur. 181182
Afyon haşhaşının tıbbi, rekreasyonel ve dini amaçlar için kullanılması, Sümer kil tabletlerindeki ideogramların bir "neşe bitkisi" olan "Hul Gil" in kullanımından bahsettiği M.Ö. dördüncü yüzyıla kadar izlenebilir. 184 Afyon Mısırlılar tarafından biliniyordu ve Ebers Papirüsü'nde çocukların yatıştırılması, ve meme apselerinin tedavisi için bir karışımda bir bileşen olarak bahsedilmektedir.
Afyon Yunanlılar tarafından da biliniyordu. Hipokrat (c. 460 – c. 370 BC) ve öğrencileri tarafından uykuya neden olan özellikleri nedeniyle değerlendirildi ve ağrı tedavisinde kullanıldı. Latince "Sedare dolorem opus divinum est", trans. "Acıyı hafifletmek ilahi olanın işidir" deyişi, Hipokrat'a ve Bergamalı Galen'e çeşitli şekillerde atfedilmiştir. Afyonun tıbbi kullanımı daha sonra Roma ordusunda görev yapan Yunan bir doktor olan Pedanius Dioscorides (MS 40 – 90 civarı) tarafından beş ciltlik eseri De Materia Medica'da tartışılmıştır.
İslami Altın Çağ boyunca, afyon kullanımı Avicenna (c. 980 – Haziran 1037 AD) tarafından The Canon of Medicine'de ayrıntılı olarak tartışılmıştır. Kitabın beş cildi afyonun hazırlanması, bir dizi fiziksel etki, çeşitli hastalıkları tedavi etmek için kullanımı, kullanımı için kontrendikasyonlar, zehir olarak potansiyel tehlikesi ve bağımlılık potansiyeli hakkında bilgi içermektedir. Avicenna, afyonun son çare olarak kullanılmasını teşvik etmedi ve analjeziklerle en aza indirmeye çalışmak yerine ağrının nedenlerini ele almayı tercih etti. İbn-i Sina'nın gözlemlerinin çoğu modern tıp araştırmaları tarafından desteklenmiştir.
Dünyanın Hindistan ve Çin'de afyonun tam olarak ne zaman farkına vardığı belirsizdir, ancak Çin tıbbi çalışması K'ai-pao-pen-tsdo'da (MS 973 gelindiğinde, afyon haşhaşları Agra Subah bölgesinde temel bir bahar ürünüdür.
Doktor Paracelsus (c. 1493-1541), Alman Rönesansı sırasında Batı Avrupa'da afyonu tıbbi kullanıma yeniden sokmakla tanınır. Afyonun tıbbi kullanım için faydalarını övdü. Ayrıca, laudanum adını verdiği bir hap olan bir "arcanum"a sahip olduğunu iddia etti, bu da özellikle ölüm aldatılacaksa, diğerlerinden daha üstündü. ("Ich hab' ein Arcanum – heiss' ich Laudanum, ist über das Alles, wo es zum Tode reichen will.") Daha sonraki yazarlar, Paracelsus'un laudanum tarifinin afyon içerdiğini, ancak kompozisyonunun bilinmediğini iddia etmişlerdir.
Laudanum
Laudanum terimi, 17. yüzyıla kadar yararlı bir ilaç için genel olarak kullanılmıştır. Thomas Sydenham, afyonun ilk sıvı tentürünü tanıttıktan sonra, "laudanum" hem afyon hem de alkolün bir karışımı anlamına geldi. Sydenham'ın 1669 laudanum tarifi, afyonu şarap, safran, karanfil ve tarçın ile karıştırdı. Sydenham'ın laudanumu 20. yüzyıla kadar hem Avrupa'da hem de Amerika'da yaygın olarak kullanılmıştır. Afyona dayanan diğer popüler ilaçlar, çocuklar için çok daha hafif bir sıvı preparat olan Paregoric'i içeriyordu; Siyah damla, daha güçlü bir hazırlık; ve Dover'ın tozu.
Afyon ticareti
Afyon, diğerlerinin yanı sıra Hindistan, Portekizliler, Hollandalılar, İngilizler ve Çin'i içeren ticaret ağları aracılığıyla yasal ve yasadışı olarak hareket eden büyük bir sömürge metası haline geldi. İngiliz Doğu Hindistan Şirketi, afyon ticaretini MS 1683'te bir yatırım fırsatı olarak gördü. Bengal Valisi, Doğu Hindistan Şirketi adına Bengal afyonu üretimi üzerinde bir tekel kurdu. Hint afyonunun ekimi ve üretimi, 1797 ve 1949 yılları arasında bir dizi eylemle daha da merkezileştirildi ve kontrol edildi. İngilizler, Çin hükûmetinin yasaklarına meydan okuyarak Çin'e kaçırılan Hint afyonunu satarak Çin çayının ithalatından kaynaklanan ekonomik açığı dengeledi. Bu, Çin ve İngiltere arasında Birinci (1839-1842) ve İkinci Afyon Savaşları'na (1856-1860) yol açtı.
Morfin
19. yüzyılda, geniş kapsamlı etkileri olan iki büyük bilimsel ilerleme kaydedildi. 1804 civarında, Alman eczacı Friedrich Sertürner, morfinleri afyondan izole etti. Kristalleşmesini, yapısını ve farmakolojik özelliklerini 1817'de iyi karşılanan bir makalede açıkladı. Morfin, modern bilimsel ilaç keşfinin başlangıcı olan herhangi bir tıbbi bitkiden izole edilen ilk alkaloiddi.
İkinci ilerleme, yaklaşık elli yıl sonra, Alexander Wood ve diğerleri tarafından hipodermik iğnenin rafine edilmesiydi. Subkutan iğneli bir cam şırınganın geliştirilmesi, birincil aktif bir bileşiğin kontrollü ölçülebilir dozlarının kolayca uygulanmasını mümkün kılmıştır.
Morfin başlangıçta ağrıyı hafifletme kabiliyeti nedeniyle harika bir ilaç olarak selamlandı. İnsanların uyumasına yardımcı olabilir, ve öksürük ve ishal kontrolü de dahil olmak üzere diğer yararlı yan etkilere sahipti. Doktorlar tarafından yaygın olarak reçete edildi ve eczacılar tarafından kısıtlama olmaksızın dağıtıldı. Amerikan İç Savaşı sırasında, afyon ve laudanum askerleri tedavi etmek için yaygın olarak kullanıldı. Ayrıca kadınlar, adet ağrısı ve "sinir karakterli" hastalıklar için sık sık reçete edildi. İlk başta (yanlışlıkla) bu yeni uygulama yönteminin bağımlılık yapmayacağı varsayılıyordu.
Kodein
Kodein 1832'de Pierre Jean Robiquet tarafından keşfedildi. Robiquet, İskoç kimyager William Gregory (1803-1858) tarafından tanımlanan morfin ekstraksiyonu için bir yöntemi gözden geçiriyordu. Gregory'nin prosedüründen kalan kalıntıyı işleyen Robiquet, afyonun diğer aktif bileşenlerinden kristalin bir maddeyi izole etti. Keşfi hakkında şunları yazdı: "İşte afyonda bulunan yeni bir madde ... Şimdiye kadar afyonun tek aktif prensibi olduğu düşünülen morfinin tüm etkileri hesaba katmadığını biliyoruz ve fizyologlar uzun süredir doldurulması gereken bir boşluk olduğunu iddia ediyorlar." Alkaloidi keşfetmesi, kodeine dayanan bir nesil antitussif ve antidiarreal ilaçların geliştirilmesine yol açtı.
Yarı sentetik ve sentetik opioidler
Sentetik opioidler icat edildi ve eylemleri için biyolojik mekanizmalar 20. yüzyılda keşfedildi. Bilim adamları bağımlılık yapmayan opioid formlarını aradılar, ancak bunun yerine daha güçlü olanları yarattılar. İngiltere'de Charles Romley Alder Wright, bağımlılık yapmayan bir afyon türevi arayışında yüzlerce afyon bileşiği geliştirdi. 1874'te, birkaç saat boyunca asetik anhidrit ile kaynatılmış morfini içeren asetilasyon adı verilen bir işlem kullanarak diamorfin (eroin) sentezleyen ilk kişi oldu.
Eroin, Bayer Laboratuvarları'nda Heinrich Dreser (1860-1924) için çalışan Felix Hoffmann (1868-1946) tarafından bağımsız olarak sentezlenene kadar çok az ilgi gördü. Dreser, yeni ilacı 1898'de tüberküloz, bronşit ve astım için analjezik ve öksürük tedavisi olarak piyasaya sürdü. Bayer, eroinin bağımlılık potansiyeli fark edildikten sonra 1913'te üretimi durdurdu.
1910'larda Almanya'da birkaç yarı sentetik opioid geliştirildi. İlki, oksimorfon, 1914'te afyon haşhaşlarında bir opioid alkaloid olan thebaine'den sentezlendi. Daha sonra, Martin Freund ve Edmund Speyer, 1916'da Frankfurt Üniversitesi'nde yine thebaine'den oksikodon geliştirdiler. 1920'de hidrokodon, Carl Mannich ve Helene Löwenheim tarafından kodeinden türetilerek hazırlandı. 1924'te hidromorfon, morfine hidrojen eklenerek sentezlendi. Etorfin, 1960 yılında afyon haşhaş samanındaki oripavin'den sentezlendi. Buprenorfin 1972 yılında keşfedildi.
İlk tam sentetik opioid, 1932'de IG Farben'de Alman kimyager Otto Eisleb (veya Eislib) tarafından tesadüfen bulunan meperidin (daha sonra demerol) idi. Meperidin, morfin ile ilgisi olmayan, ancak afyon benzeri özelliklere sahip bir yapıya sahip ilk afyondu. Analjezik etkileri 1939'da Otto Schaumann tarafından keşfedildi. Yine IG Farben'de bulunan Gustav Ehrhart ve Max Bockmühl, Eisleb ve Schaumann'ın çalışmaları üzerine inşa edildi. 1937 civarında "Hoechst 10820" (daha sonra metadon) geliştirdiler. 1959'da Belçikalı doktor Paul Janssen, eroinin gücünün 30 ila 50 katı olan sentetik bir ilaç olan fentanil geliştirdi. Şu anda yaklaşık 150 sentetik opioid bilinmektedir.
Kriminalizasyon ve tıbbi kullanım
Afyonun klinik olmayan kullanımı, Amerika Birleşik Devletleri'nde 1914 Harrison Narkotik Vergi Yasası ve diğer birçok yasa tarafından suç sayılmıştır. Opioidlerin kullanımı damgalandı ve ölmekte olan hastalar için sadece son çare olarak reçete edilmesi tehlikeli bir madde olarak görüldü. 1970 tarihli Kontrollü Maddeler Yasası sonunda Harrison Yasası'nın sertliğini hafifletti.
Birleşik Krallık'ta, Kraliyet Hekimler Koleji Başkanı'nın başkanlığındaki Morfin ve Eroin Bağımlılığı Bölüm Komitesi'nin 1926 tarihli raporu, tıbbi kontrolü yeniden ileri sürdü ve 1960'lara kadar süren "İngiliz kontrol sistemini" kurdu.
1980'lerde Dünya Sağlık Örgütü, farklı ağrı seviyeleri için opioidler de dahil olmak üzere ilaçların reçete edilmesi için kılavuzlar yayınladı. ABD'de, Kathleen Foley ve Russell Portenoy, opioidlerin "inatçı malign olmayan ağrı" vakaları için ağrı kesici olarak liberal kullanımının önde gelen savunucuları oldular. İddialarını destekleyecek çok az bilimsel kanıt veya hiç bilimsel kanıt olmadan, endüstri bilim adamları ve savunucuları kronik ağrısı olan kişilerin bağımlılığa karşı dirençli olacağını öne sürdüler.
1996 yılında OxyContin'in piyasaya sürülmesine, ağrı kesici için opioidlerin kullanımını teşvik eden agresif bir pazarlama kampanyası eşlik etti. Opioidlerin reçetelenmesinin artması, eroin için büyüyen bir karaborsayı körükledi. 2000 ve 2014 yılları arasında "ülke genelinde eroin kullanımında endişe verici bir artış ve aşırı dozda uyuşturucu ölümleri salgını" yaşandı. 224
Sonuç olarak, sağlık kuruluşları ve Sorumlu Opioid Reçeteleme Hekimleri gibi halk sağlığı grupları, opioidlerin reçetelenmesinde azalma çağrısında bulunmuştur. 2016 yılında, Hastalık Kontrol ve Önleme Merkezleri (CDC), opioidlerin "aktif kanser tedavisi, palyatif bakım ve yaşam sonu bakımı dışındaki kronik ağrı için" reçetelenmesi ve opioid sivrilmesinin artması için yeni bir dizi kılavuz yayınladı.