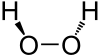Hidrojen peroksit
| Hidrojen peroksit | |
|---|---|
|
Hydrogen peroxide
| |
|
Diğer adlar
Perhidroksik asit
Dihidrojen dioksit Oksijenli su | |
| Tanımlayıcılar | |
| CAS numarası | 7722-84-1 |
| PubChem | 784 |
| UN numarası | 2015 (>60% çözelti) 2014 (20–60% çözelti) 2984 (8–20% çözelti) |
| ChEBI | 16240 |
| RTECS numarası | MX0900000 (>90% çözelti) MX0887000 (>30% çözelti) |
| SMILES |
|
| ChemSpider | 763 |
| Özellikler | |
| Molekül formülü | H2O2 |
| Molekül kütlesi | 34.0147 g/mol |
| Görünüm | Soluk mavi; sulu çözeltisi renksiz |
| Koku | Hafif keskin |
| Yoğunluk | 1.11 g/cm3 (20 °C, 30% (w/w) çözelti) 1.45 g/cm3 (20 °C, Saf) |
| Erime noktası |
−0.43 °C (31.23 °F; 272.72 K) |
| Kaynama noktası |
150.2 °C (302.4 °F; 423.3 K) (ayrışır) |
| Çözünürlük () |
Eter ve alkolde çözünür petrol eterinde çözünemez |
| log P | -0.43 |
| Buhar basıncı | 5 mmHG (30 °C) |
| Asitlik (pKa) | 11.75 |
| Akmazlık | 1.245 cP (20 °C) |
| Tehlikeler | |
| GHS piktogramları |
  
|
| NFPA 704 | |
| Parlama noktası | Yanmaz |
| Belirtilmiş yerler dışında verilmiş olan veriler, Standart sıcaklık ve basınçtadır. (25 °C, 100 kPa) | |
| Bilgi kutusu kaynakları | |
Hidrojen peroksit (H2O2), saf haldeyken oldukça açık mavi renkte; sulandırıldığında ise renksiz hale gelen bir bileşiktir. Viskozitesi sudan daha yüksek olan ve zayıf asidik özellik gösteren bileşik, aynı zamanda güçlü bir oksitleyicidir. Özellikle tıp alanında %3'lük sulu çözeltisi ve kâğıt sanayiinde kâğıtlara beyaz renk vermek için kullanılmaktadır. Bileşik ayrıca dezenfektasyon, oksitleme, antiseptik üretimi ve roket yakıtı üretiminde de tercih edilir.
İnsan vücudunda bu molekülü parçalamak üzere karaciğerde üretilen katalaz adlı bir enzim yer almaktadır. Bu enzim, hidrojen peroksit molekülünü parçalayarak su ve oksijen molekülü eldesi sağlar.
Tarihi
Hidrojen peroksit ilk defa 1818 yılında Fransız kimyacı Louis Jacques Thénard tarafından baryum peroksitin nitrik asit ile tepkimeye sokulmasıyla elde edilmiştir. Üretildikten sonra, uzun süre boyunca bileşiğin kararsız olduğuna inanıldı. 19. yüzyılın sonunda Petre Melikishvili ve öğrencisi L. Pizarjevski bileşiğin doğru formülünün H-O-O-H şeklinde olduğunu gösterdi.